-- 论临床试验设计的重要性
近日,药渡发布了题为《Challenge the best-中国Biotech走向国际,系列报道(二)-- 论临床试验设计的重要性 》的文章,原文内容如下:
在当前国内创新药研发追赶国际领先水平的过程中,临床试验已成为决定成败的关键。近日康乃德生物医药有限公司宣布CBP-307治疗中重度溃疡性结肠炎2期临床试验的12周顶线结果,在临床缓解率(FDA和CDE均认可的药物审批指标)和其他次要终点方面达到了统计学意义,并且显示出有效下调淋巴细胞数的药理活性,且CBP-307总体上显示出良好的耐受性。但主要疗效终点-试验组与基线相比“改良Mayo评分”的改善幅度未达到统计学意义。药渡参考同类药物研发进展和国外主流投行的评论,更为深入和客观地对其结果进行了解读。
前言
溃疡性结肠炎(UC)是一种累及结肠黏膜和黏膜下层的连续性、倒灌性、非特异性的慢性肠道炎性疾病,临床表现为持续或反复发作的腹泻、黏液脓血便伴腹痛和不同程度的全身症状,病程多在4~6周以上,可大大降低个人的生活质量。UC复发率高,临床表现变异性大,有统计称近50%患者需要住院治疗。据估算全球UC药物市场已超过75亿美元,占免疫市场总量的10%,预计到2026年UC药物市场将达到110-120亿美元。
近年来我国UC报告病例明显增加,正逐渐成为常见的肠道疾病和慢性腹泻的主要病因,预计我国UC患病率会逐步接近西方国家(>40/10万人)。UC病因尚不明确,暂无法治愈,国内以氨基水杨酸类和类固醇激素类药物治疗为主,免疫抑制剂应用较少。
鉴于显著的未满足临床需求,国内外都在积极探索多种靶向治疗方法,主要的靶点和机制包括:选择性S1P受体调节剂、Janus激酶(JAK)3抑制剂、人白细胞介素(IL)-12,IL-22,IL-23和IL-36抑制剂及二氢乳清酸脱氢酶(DHODH)抑制剂等。其中BMS(原Receptors公司)的选择性S1P受体调节剂Ozanimod于2020年被FDA和EMA批准上市,辉瑞(原Arena Pharmaceuticals公司)的Etrasimod不久前刚完成一项临床3期研究,两者相关的收购交易金额均超过60亿美元,印证了这类药物的巨大潜力。
在UC治疗药物的临床研究中,基于改良Mayo评分(评估大便频率、直肠出血和内窥镜检查评分)和完整Mayo评分(在改良Mayo评分基础上加入医生整体评估)的临床缓解率,是FDA和CDE认可的注册审批主要疗效终点,也是支持早前获批治疗UC药物的临床试验中的主要疗效终点。
CBP-307临床结果解读
CBP-307是康乃德基于自主专有的免疫调节技术发现的小分子口服1-磷酸鞘氨醇受体1(S1P1)调节剂,作用机制如下图:
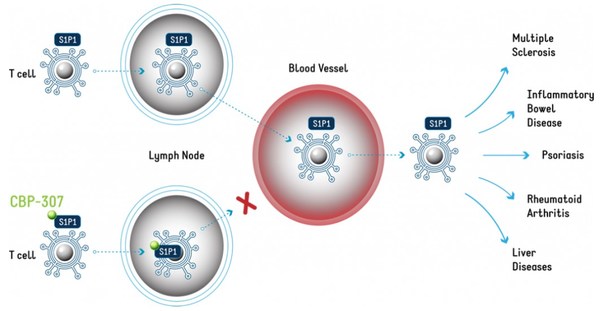
来源:康乃德官网
S1P1介导T细胞从淋巴结迁出进入外周血液循环,从而活性T细胞可迁移到组织中释放炎症介质。CBP-307 诱导 T 细胞表面的S1P1内化,将 T 细胞困在淋巴结内,阻止其迁移到炎症部位,从而达到减轻炎症的目的。
CBP-307CN002是一项进行中的2期研究,旨在评估CBP-307作为诱导和维持治疗中重度成年UC患者的有效性和安全性。这项随机、双盲、安慰剂对照、多中心研究共入组了145例受试者,研究有两个剂量活性药物组(CBP-307 0.1 mg [n=39];CBP-307 0.2 mg [n=53])和一个安慰剂组(n=53),受试者来自4个国家的60多个研究中心。目前还在继续2期UC试验维持治疗和安全性随访,本次发布的是第一阶段12周顶线结果,药渡的解读如下:
CBP-307临床结果积极,抖客网,临床缓解率(FDA及CDE批准上市的关键指标)已达到预期
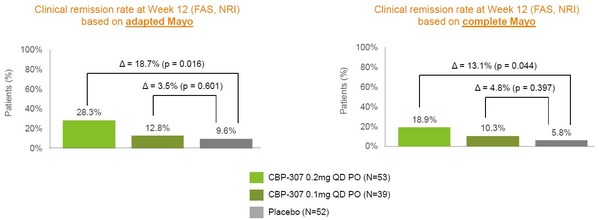
来源:康乃德官网
由上图可见,在基于改良和完整Mayo评分两方面,0.2mg CBP-307组与安慰剂组相比都达到了更高的临床缓解率,且具有统计学意义。若能在3期研究中延续这一趋势,足以达到上市审批的要求。
至于容易引起争议的主要疗效终点-改良Mayo评分较基线的最小二乘(LS)均值变化,确实未达到统计学意义,详见下图(左侧),但如果基于完整Mayo评分(右侧),则具有显著的统计学差异。
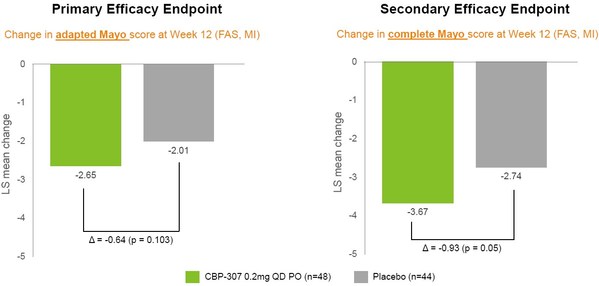
来源:康乃德官网
药渡注意到该研究安慰剂组的评分变化幅度较大(-2.01和-2.74),大于同类主要竞品Etrasimod在相关临床研究中的数值(-1.5和-2.08),这对结果统计造成了一定的影响。
据不完全统计,在我国中度UC患者比例超过40%,重度患者约20%。对于创新的口服S1P1调节剂,出于谨慎的考虑,国内临床试验执行过程中往往倾向于纳入中度的患者而非重度,可能存在一定的选择偏倚,造成基线变化幅度较大;后续研究中如果能够增加入组患者数,或者增加重度患者的比例,可能会得到更显著的疗效差异。
另外,Ozanimod和Etrasimod的相关临床试验中,入组患者的平均患病年限更长(>6年),在Mayo评分上可能更高,从而具有基线差异,因此临床试验中的评分下降幅度可能相较于CBP-307更多。
本次试验人群中亚洲人占比较高(0.2mg CBP-307组为48/53,90.6%),参考以往其它竞品所开展的研究,欧美和亚裔UC患者的临床数据是有差异的:维多珠单抗的3期研究中,日本患者安慰剂组的临床缓解和应答显著高于全球患者,导致日本受试者给药组的数据表现不如全球患者;英夫利昔单抗的3期研究中,中国患者的疾病年限相较全球要短1-2年,安慰剂组方面中国受试者的应答率等也较全球更高。因此药渡推测未来如果纳入更多欧美患者有望得到更好的统计学数据。
Fierce Biotech、Bioworld、Jefferies和SVB Leerink等国外专业机构均认可本次披露的临床结果展示出了CBP-307能够带来较好的临床获益,Jefferies还指出本次试验获得的缓解率若经安慰剂校正可能好于同靶点的其它竞品。另外,国内外相关知名IBD临床研究PI也基本认可CBP-307目前显示出的有效性和安全性。尽管临床2期primary endpoint的选择对结果的解读造成了一些影响,但应该不会被要求重新进行临床试验,预计未来继续推进3期临床研究也不会有问题(业界不乏曾经遇到阶段性临床结果与首要终点预期不符,但通过优化后续关键性临床试验设计最终顺利获批的例子,如吉非替尼、纳武利尤单抗等)。
Piper Sandler在上个月曾专门发文回顾了CBP-307临床前和临床I期的数据,CBP-307对S1P1的活性(EC50)最强(与主要竞品相比),对S1P4和S1P5的效力明显低于S1P1,对S1P3(已知有安全问题的受体亚型)基本没有活性。更低的剂量下即可实现较强的淋巴细胞计数抑制,且停药后淋巴细胞恢复更快(<7d),与同类产品所公开的数据相比,CBP-307明显缩短了治疗停药后免疫力恢复的时间,从而可降低患者感染的风险。
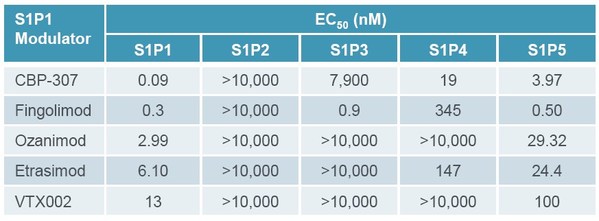
来源:Piper Sandler
|
原标题:【药渡:Challenge the best-中国Biotech走向国际】 内容摘要:-- 论临床试验设计的重要性 近日, 药渡发布了题为《Challenge the best-中国Biotech走向国际,系列报道(二)-- 论临床试验设计的重要性 》的文章,原文内容如下 : 在当前国内创新药研发追赶 ... 文章网址:https://www.doukela.com/zmt/84422.html; 免责声明:抖客网转载此文目的在于传递更多信息,不代表本网的观点和立场。文章内容仅供参考,不构成投资建议。如果您发现网站上有侵犯您的知识产权的作品,请与我们取得联系,我们会及时修改或删除。 |



